- 417.00 KB
- 52页
- 1、本文档共5页,可阅读全部内容。
- 2、本文档由网友投稿或网络整理,如有侵权请及时联系我们处理。
'第十三章分光光度法
利用物质对光的选择性吸收,可进行定性分析和定量分析。一定波长下,被测溶液对光的吸收程度与溶液中组分的浓度之间存在定量关系,可进行该组分的含量测定,该定量测定方法称为吸光光度法。
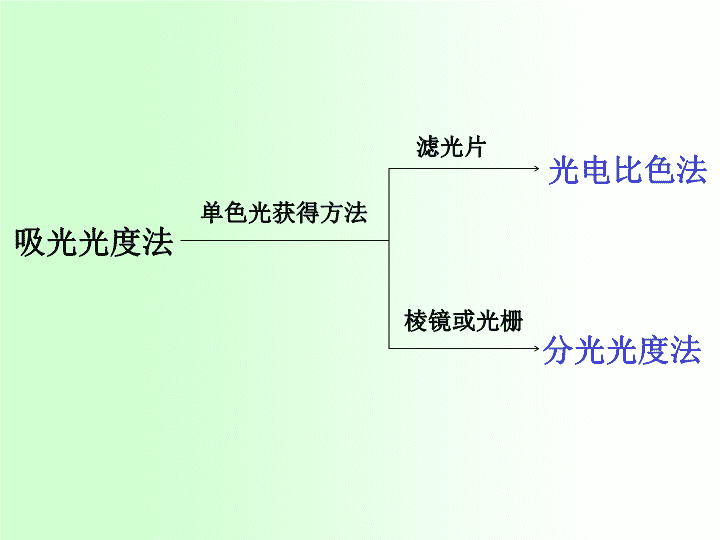
吸光光度法单色光获得方法滤光片棱镜或光栅光电比色法分光光度法
▲红外分光光度法:吸收光波长范围2.51000m,主要用于有机化合物结构鉴定。▲紫外分光光度法:吸收光波长范围200400nm(近紫外区),可用于结构鉴定和定量分析。▲可见分光光度法:吸收光波长范围400750nm,主要用于有色物质的定量分析。依物质对不同波长范围光的吸收,主要有:
第一节物质对光的选择性吸收1光的基本性质上式表明光的波长越短,或者说频率越大,光的能量越高。光是一种电磁波,具有波粒二象性,即波动性、粒子性。(Planck常数:h=6.63×10-34J·S)
●日常生活中肉眼所见到的白光,如日光等是由红、橙、黄、绿、青、蓝、紫等光按适当的强度比例混合而成的,是在400~750nm范围的一种复合光。●具有同一波长的光称为单色光。(由具有相同能量的光子组成)●不同波长组成的光称为复合光。
2物质对光的选择性吸收光的互补两种颜色的光若按适当比例混合,可以形成白光,这两种光称为互补色光。
实验证明:溶液的颜色是由于溶液中的有色物质吸收了某一波长的光所造成的。如KMnO4吸收绿色光,因此KMnO4溶液呈现紫色。白光青蓝青绿黄橙红紫蓝互补色光
◆物质的分子具有不连续的量子化能级,见图13-1双原子分子的能级示意图。◆同一电子能级(A或B)中有几个振动能级(V),而同一振动能级中有几个转动能级(J),电子能级间的能量差一般为1~20电子伏特(eV)。
◆当光子的能量=电子能级间的能量差,此能量的光被物质吸收,使分子由基态跃迁到激发态,由于激发态的分子不稳定,很短的时间内又回到基态,在这个过程中,物质所吸收的能量以热或光的形式释放出来。◆由电子能级跃迁而产生的吸收光谱位于紫外及可见光部分,称为分子的电子光谱。
一束平行单色光照射溶液时,光的一部分被吸收,一部分透过溶液,一部分被器皿的表面反射。透光率T与吸光度A光通过溶液示意图ItIo=It+IaIaL
Io=It+Ia+Ir若入射光强度为Io,吸收光的强度为Ia,透过光强度为It,反射光的强度为Ir,它们的关系是Io=It+Ia在吸光光度法中,测定时都是采用同样材质的比色皿,反射光的强度基本上是不变的,约占4%,其影响可以相互抵消,上式可简化为:
溶液的透光度越大,说明对光的吸收越小,浓度低;相反,透光度越小,溶液对光的吸收越大,浓度高。透过光强度It与入射光强度Io之比称为透光度或透光率。用T表示:
若光全部透过溶液,Io=It,A=0若全部被吸收,It=0,A=∞吸光度A是用来衡量溶液中吸光物质对单色光λ的吸收程度,A值越大,其吸收程度越大;反之亦然。吸光度A
将不同波长的光依次透过某浓度一定的溶液,测量不同波长下溶液对光的吸光度,用A~λ作图KMnO4溶液的吸收曲线吸收曲线
(1)同一种物质对不同波长光的吸光度不同。吸光度最大处对应的波长称为最大吸收波长λmax。(2)不同浓度的同一种物质,其吸收曲线形状相似、λmax不变。而对于不同物质,它们的吸收曲线形状和λmax均不同。可作为物质定性分析的依据之一。有关吸收曲线:
(3)不同浓度的同一种物质,在某一定波长下吸光度A有差异,在λmax处吸光度A的差异最大。此特性可作为物质定量分析的依据。(4)在λmax处吸光度随浓度变化的幅度最大,所以测定最灵敏。吸收曲线是定量分析中选择入射光波长的重要依据。
3分光光度法特点●灵敏度高,常测10–3%~1%的微量组分,有时,10–5%~10–4%的痕量组分;适用于微量分析。●准确度较高,相对误差为2%∼5%。●快速简便。●应用广泛。
第二节光的吸收定律1朗伯-比耳定律◆1760年朗伯(Lambert)阐明了光的吸收程度和吸收层厚度的关系。A∝L◆1852年比耳(Beer)又提出了光的吸收程度和吸收物浓度之间也具有类似的关系。A∝c
数学表达式:朗伯—比尔定律:一束平行单色光通过溶液时,溶液的吸光度A与溶液的浓度c和液层厚度b成正比。K为常数,表示物质对光的吸收能力,与吸光物质的本性,入射光的波长及温度等因素有关,与浓度c无关,数值随c选择的单位变化。
2吸光系数和摩尔吸光系数(1)吸光系数aA=acL当c用g·L-1表示,L用cm表示时,K用a表示,称为吸光系数,单位为L·g-1·cm-1,则:(2)摩尔吸光系数ε当c用mol·L-1表示,L用cm表示时,K用ε表示,称为摩尔吸光系数,单位为L·mol-1·cm-1。
(1)ε不随浓度c和液层厚度L的改变而改变。在温度和波长等条件一定时,仅与吸收物质本身的性质有关,与待测物浓度无关;有关摩尔吸光系数ε
(2)同一吸光物质在不同波长下的ε值是不同的。在最大吸收波长λmax处的摩尔吸光系数,常以εmax表示。εmax表明了该吸收物质最大限度的吸光能力,也反映了光度法测定该物质可能达到的最大灵敏度。由于ε值与入射光波长有关,故表示ε时,应注明入射光波长。
(3)εmax越大表明该物质的吸光能力越强,用光度法测定该物质的灵敏度越高。ε<104反应灵敏度低104<ε<5×104反应灵敏度中5×104<ε<105反应灵敏度高ε>105反应灵敏度超高
(4)ε在数值上等于浓度为1mol·L-1、液层厚度为1cm时该溶液在某一波长下的吸光度。显然,不能直接取1mol·L-1这样高浓度的有色溶液去测量,而只能通过计算求得。
例有一浓度为1.0g·mL-1Fe2+的溶液,以邻二氮菲显色后,在比色皿厚度为2cm、波长510nm处测得吸光度为0.380,计算(1)透光率T;(2)吸光系数a;(3)摩尔吸光系数。解:(1)T=10-A=10-0.380=0.417(2)(3)
练习现有25.5g/50mL的Cu2+溶液,用双环已酮草酰二腙光度法进行测定,波长600nm处用2cm比色皿进行测量,测得T为50.5%,求摩尔吸光系数。(600)=L·mol-1·cm-1解:A=-lgT=εcL
3偏离朗伯-比耳定律的原因cA标准曲线正误差负误差①溶液本身的化学和物理因素引起的偏离。◆介质不均匀性引起的。当被测试液是胶体溶液,乳浊液或悬浮物质时,入射光中有部分因散射而损失,而使实测吸光度增加。
◆溶液中的化学反应引起的。溶液中的吸光物质常因离解、缔合、形成新化合物或互变异构等化学变化而改变其浓度,导致偏离。②由于非单色光引起的偏离严格来说,朗伯—比耳定律只适用于单色光,但我们用各种方法所得到的入射光,实质上都是复合光(物质对不同波长光的吸收程度不同),因而导致偏离。实际工作中,选择吸光物质的最大吸收波长的光为入射光。
第三节分光光度计(1)光源:应有足够的发射强度而且稳定,如钨丝灯、氘灯等。(2)单色器:采用棱镜或光栅获得单色光。(3)吸收池:比色皿,厚度有0.5、1、2、3cm等。(4)检测器:硒光电池、光电管和光电倍增管。光源单色器检测系统吸收池
第四节分析条件选择1反应条件的选择1.1显色反应使试样中的被测组分与化学试剂作用生成有色化合物的反应叫显色反应。mX(待测物)+nR(显色剂)=XmRn(有色化合物)显色反应主要有配位反应和氧化还原反应,其中绝大多数是配位反应。
1.2对显色反应的要求(1)灵敏度高,选择较大(104~105)的显色反应。避免共存组分干扰。(2)选择性好,显色剂只与被测组分反应。(3)有色物组成固定,如:Fe3++磺基水杨酸→三磺基水杨酸铁(黄色)(组成固定)Fe3++SCN-→FeSCN2+、Fe(SCN)2+……(组成不固定)
(4)有色物稳定性高,其它离子干扰才小。如三磺基水杨酸铁的Kf=1042,F-、H3PO4对它无干扰。(5)色差大。有色化合物与显色剂之间的颜色差别要大,显色时颜色变化鲜明。
1.3显色条件的选择(1)显色剂用量,适当过量。M+R=MRc(R)Ac(R)Ac(R)A
(2)溶液的酸度a影响显色剂的平衡浓度和颜色因,可见增加H+浓度,不利于显色反应。且显色剂具有酸碱指示剂的性质,不同的酸度下有不同的颜色。
b影响被测金属离子的存在状态当溶液酸度降低时,大部分金属离子在水中可能形成一系列氢氧基或多核氢氧基配离子。若酸度更低,可进一步水解生成碱式盐或氢氧化物沉淀。c影响配合物的组成对于某些生成逐级配合物的显色反应,酸度不同,配合比往往不同,颜色也不同。
要找到显色反应的适宜酸度,通常是经实验确定的。固定溶液中被测组分与显色剂的浓度,调节不同的pH值,测A,作pH—A曲线图,找适宜pH值。
绘制吸光度—温度曲线加以确定(4)显色温度(3)显色时间用实验方法确定。配制一份显色溶液,以加入显色剂的时间开始,每隔几分钟测一次吸光度,绘制吸光度—时间曲线图,确定适宜的显色时间。
2仪器测量条件的选择(1)入射光的波长的选择(545nm)K2Cr2O7-KMnO4吸收曲线吸收最大,干扰最小。
(2)吸光度计数范围的选择根据朗伯—比耳定律及误差传递公式可推出下列结果:当T=36.8%即A=0.4343时,浓度测量的相对误差最小。一般来说,适宜的吸光度范围:T=15%~65%A=0.2~0.8
3参比溶液的选择测吸光度时,利用参比溶液调节T=100%(即调节仪器的零点),以消除误差。(1)溶剂参比试样、试剂、显色剂均无色(2)试剂参比试样无色、试剂或显色剂有色(3)试样参比试样有色、试剂和显色剂均无色
第五节定量方法1单组分定量方法1.1标准曲线法配制一系列不同含量的标准溶液,以不含被测组分的空白为参比,在相同条件下,测定标准溶液的吸光度,绘制吸光度—浓度曲线,称之为标准曲线。cA标准曲线Axcxc1c2c3c4c5A1A2A3A4A5
1.2标准对照法同条件下分别测定未知液与标准溶液的吸光度Ax和As,根据朗伯-比尔定律,应有下式:
2多组分定量方法在多组分体系中如果各吸光物质之间无相互作用这时体系总的吸光度等于各个吸光物质的吸光度之和。
(a)组分x、y互不干扰,可分别在λ1和λ2处测溶液的吸光度。
(b)x干扰y,而y对x无干扰。可先在λ1处测溶液吸光度,求出x组分的浓度cx。再在λ2处测(溶液吸光度),纯组分x和y的、则:
(c)x、y相互干扰。
3示差分光光度法示差分光光度法:采用一个比被测试液浓度稍低的标准溶液作参比溶液,调节T为100%(A=0)。设参比溶液浓度为cs,被测溶液浓度cx,则:两式相减:
两溶液的吸光度差△A与浓度差△c成正比。标准溶液c1、c2、c3……。以c1作参比,调A=0。测c2、c3……的△A,用△A对△c作图。同条件下测△Ax,从示差工作曲线中查出△cx。cx=△cx+c1△A△c△Ax△cx示差工作曲线
练习采用邻二氮菲法测定铁。称取试样0.5585g,经处理后加入显色剂,定容为50.00mL,用厚度为1cm的比色皿在λmax=510nm处测得吸光度A=0.400。试计算该样品中铁的百分含量。如果把溶液稀释一倍,透光率是多少?(ε570=1.0×104L·mol-1·cm-1,MFe:55.85)
解:A=εcL=ω=A=-lgT=εcL=-lgTT=10-0.200=63.1%
练习测得浓度为6μg·mL-1Fe3+标准溶液的T=60%。在同一条件下,测得试样溶液的T=80%,求试样Fe3+的含量(μg·mL-1)。解:根据朗伯比尔定律A=-lgT=εcL-lg0.60=εL·6-lg0.80=εL·cc='
您可能关注的文档
- 第五章紫外可见分光光度法.ppt
- 7可见分光光度法.ppt
- 采用分光光度法测定弱电解质的电离常数实验报告.doc
- GBT 17141-1997 土壤质量 铅、镉的测定 石墨炉原子吸收分光光度法.doc
- 固定污染源排气中氯化氢的测定 硫氰酸汞分光光度法HJT27-1999方法确认.doc
- 可见—紫外分光光度法测定浓度.doc
- 水质 铁、锰的测定 火焰原子吸收分光光度法.docx
- 紫外-可见分光光度法00.doc
- 紫外分光光度法.doc
- 分光光度法补充1.ppt
- 分光光度法测定水中总铁.ppt
- 第六章 分光光度法.ppt
- 邻二氮菲分光光度法测定微量铁.ppt
- 第九章荧光分光光度法.ppt
- 第四章 紫外-可见分光光度法.ppt
- 紫外-可见分光光度法.ppt
- 紫外分光光度法.ppt
- 第十三章 可见分光光度法和紫外分光光度法.ppt