- 2.44 MB
- 73页
- 1、本文档共5页,可阅读全部内容。
- 2、本文档由网友投稿或网络整理,如有侵权请及时联系我们处理。
'第四章紫外-可见
分光光度法
学习目标1.掌握紫外-可见分光光度法的原理;2.熟悉紫外-可见分光光度计的结构及各部分作用,了解不同类型分光光度计的结构;3.了解紫外-可见分光光度法实验条件的选择;4.掌握紫外-可见分光光度计的定性定量方法。
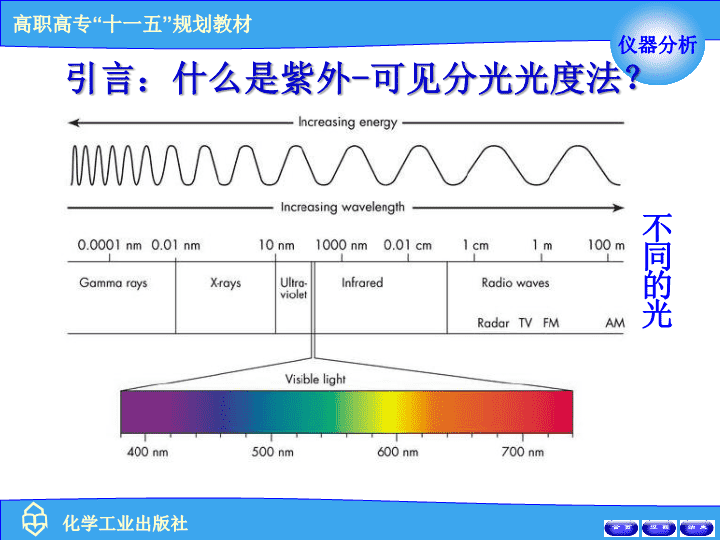
引言:什么是紫外-可见分光光度法?是根据物质分子对波长为200-760nm这一范围的电磁波的吸收特性所建立起来的一种定性、定量和结构分析方法。不同的光
主要内容§4.1基本原理§4.2紫外-可见分光光度计§4.3分析条件的选择§4.4紫外-可见分光光度法的应用
§4.1基本原理透光率和吸光度郎伯-比尔定律吸光系数吸收光谱基本原理光的吸收定律偏离郎伯-比尔定律的因素摩尔吸光系数百分吸光系数
1.透光率一、透光率和吸光度用透光率T表示透射光所占的比例大小:
2.吸光度A表示物质对光的吸收程度。吸光度A的公式:吸光度A与透光率T变化相反,吸光度愈大,物质的吸光能力越强一、透光率和吸光度
二、郎伯-比尔定律(一)光的吸收定律当一束平行的单色光通过某一均匀、无散射的含有吸光物质的溶液时,在入射光的波长、强度以及溶液的温度等因素保持不变的情况下,该溶液的吸光度A与溶液的浓度C及溶液层的厚度l的乘积成正比关系。称为郎伯-比尔定律:
(一)光的吸收定律吸光度具有加和性,即如果溶液中同时存在多种吸光物质,那么,测得的吸光度则是各吸光物质吸光度的总和。其表达式为:二、郎伯-比尔定律
(二)偏离郎伯-比尔定律的因素根据郎伯-比尔定律,如固定液层厚度l,以吸光度对浓度作图时,应得到一条通过原点的直线。但在实际工作中,吸光度与浓度之间的线性关系常常发生偏离二、郎伯-比尔定律
1.非单色光的影响在紫外-可见分光光度计中,由于仪器性能的限制,得到的不是严格的单色光。2.非均相体系的影响当样品溶液中含有颗粒等悬浮杂质时,样品为不均匀的体系,光线会出现散射。(二)偏离郎伯-比尔定律的因素
3.溶液本身发生化学变化的影响溶液中待测组分发生了解离、缔合、光化等作用,造成物质光学性质改变,偏离了郎伯-比尔定律。例如,铬酸盐在溶液中有如下平衡:Cr2O72-呈橙色,而CrO42-呈黄色,两者对不同波长光线的吸收性能完全不同。(二)偏离郎伯-比尔定律的因素
4.浓度的限制朗伯-比尔定律假定吸光质点之间不发生相互作用,因此只有在稀溶液时才基本符合。浓度较高时,质点之间会互相影响对方的电荷分布,吸光性能发生改变,必然导致偏离郎伯-比尔定律。(二)偏离郎伯-比尔定律的因素
三、吸光系数吸光系数k的物理意义为:液层厚度为1cm的单位浓度溶液的吸光度,它表示物质对特定波长光的吸收能力。一个物质在一定条件下的吸光系数为定值。通常有两种表示方法:摩尔吸光系数ε百分吸光系数吸光系数k
物理意义是指样品浓度为1mol·L-1的溶液置于1cm样品池中,在一定波长下测得的吸光度值。量纲为L·mol-1·cm-1。ε104102中强吸收弱吸收强吸收(一)摩尔吸光系数ε
(二)百分吸光系数物理意义是指溶液浓度在1%(1g/100mL),液层厚度为1cm时,在一定波长下的吸光度值。量纲为100mL·g-1·cm-1。百分吸光系数和摩尔吸光系数有如下关系:
例4-1用氯霉素(分子量为323.15)纯品配制100mL含2.00mg的溶液,使用1.00cm的吸收池,在波长为278nm处测得其透射率为24.3%,试计算氯霉素在278nm波长处的摩尔吸光系数和比吸光系数。解:已知λ=278nmM=323.15g/molc=2.00×10-3%T=24.3%三、吸光系数
四、吸收光谱
不同浓度KMnO4溶液的吸收光谱四、吸收光谱
§4.2紫外-可见分光光度计
一、基本构造基本结构由五部分组成光源单色器吸收池检测器信号处理系统
1.光源用于提供分析所需的光线类型实例光谱范围热辐射光源钨灯、碘钨灯320~2500nm提供可见光区光源气体放电光源氢灯、氘灯160~375nm提供紫外光区光源一、基本构造
2.单色器又称为分光系统,是从复合光中分出单色光的光学装置。有狭缝,透镜,色散元件等部件。其中,色散元件最为重要,常见的有棱镜和光栅单色器透镜狭缝色散元件光栅棱镜一、基本构造
2.单色器单色器几大部件的示意图棱镜式光栅式一、基本构造
3.吸收池用于盛放溶液的装置。又称比色皿。分为两种材质:石英或者玻璃不同材质比较吸收池材质特点适用范围玻璃吸收紫外线强不能用于紫外光区测定石英吸收紫外线弱可见光区、紫外光区均可使用一、基本构造
3.吸收池厚度不一的石英吸收池一、基本构造
4.检测器把光信号转变为电信号的装置例如:光电管、灵敏度较高的光电倍增管等;5.信号处理系统记录信号并进行处理的装置例如:连接在仪器上的微型计算机一、基本构造
二、常见紫外-可见分光光度计类型③双波长分光光度计①单波长单光束分光光度计②单波长双光束分光光度计光度计类型
1.单波长单光束分光光度计由一束单色光依次通过样品池和参比池二、常见紫外-可见分光光度计类型
2.单波长双光束分光光度计一束光分为强度相等的两束,分别通过样品池和参比池二、常见紫外-可见分光光度计类型
3.双波长分光光度计用两不同波长的单色光交替通过吸收池,利用不同波长处吸光度的差值进行测定,无需参比池。二、常见紫外-可见分光光度计类型
§4.3分析条件的选择分析条件的选择测量波长狭缝宽度吸光度的范围仪器条件的选择显色剂反应的要求显色条件的选择溶剂参比溶液试剂参比溶液样品参比溶液平行操作参比溶液参比溶液显色条件选择
一、仪器条件的选择(一)测量波长通常选择最强吸收峰的最大吸收波长λmax为入射波长。在该波长处,吸收度大,灵敏度较高。如在该波长有干扰,可选次强吸收峰的最大吸收波长λmax为吸收波长
(二)狭缝宽度狭缝宽度变宽光线谱带变宽;光线强度增加变窄光线谱带变窄;光线强度减弱灵敏度↓↑↓↑通常选在不减少吸光度时的最大狭缝宽度为适宜的狭缝宽!一、仪器条件的选择
(三)吸光度的范围当吸光度A在0.3~0.7范围内时,实验的测量误差较小。通常实验时,将吸光度的测量范围控制在0.2~0.8内。一、仪器条件的选择
如果待测组分本身没有颜色或本身颜色很浅,那么就无法直接进行测定,需利用显色反应将待测组分转变为有色物质,然后进行测定。这种将试样中待测组分转变成有色化合物的化学反应,叫显色反应。与待测组分形成有色化合物的试剂叫显色剂。二、显色条件的选择
例如:Fe2+本身颜色很弱。如加入显色剂邻二氮菲,则生成稳定橙红色络合物,该络合物吸光能力强,用于含量测定效果佳。二、显色条件的选择
(一)显色剂反应的要求1.显色反应灵敏度高显色反应产物的ε愈大,灵敏度愈高;2.显色剂选择性高显色剂应尽量只与待测组分反应,而不与溶液中其他共存组分反应。二、显色条件的选择
(一)显色剂反应的要求3.显色剂的对照性要高显色剂的颜色应与显色反应产物的颜色有较大区分,使实验结果更为准确;4.显色产物稳定显色反应产物应有一定的稳定性。二、显色条件的选择
(二)显色条件的选择1.显色剂浓度及用量最适宜显色剂浓度及用量可通过实验确定。2.溶液pH显色剂一般本身为弱酸或弱碱,溶液的pH值可显著影响显色剂的解离程度和显色反应的完成程度。可通过实验确定最合适pH。二、显色条件的选择
(二)显色条件的选择3.显色反应的时间和温度显色反应一般需要一定时间,显色程度会随着时间变化而变化。可作显色反应时间-吸光度曲线,最合适的时间为曲线中的平坦部分二、显色条件的选择
(二)显色条件的选择3.显色反应的时间和温度显色温度通常选在室温下进行,有的显色反应发生较慢,可适当升高温度。灵芝多糖溶液加入显色剂后的时间-吸光度曲线二、显色条件的选择
三、参比溶液紫外-可见分光光度法需要参比溶液作空白以消除吸收池壁、溶剂对入射光的反射和吸收所带来的误差及其他一些干扰因素所带来的影响。要视具体情况选择合适的参比溶液。
1.溶剂参比溶液当样品简单,无显色剂或显色剂无吸收,直接用溶剂作参比溶液。2.试剂参比溶液对于显色反应,显色剂如有吸收,可在溶剂中加入与样品溶液相同含量的显色剂的溶液作参比溶液。三、参比溶液
3.样品参比溶液对于样品较为复杂的显色反应,可用不加显色剂的样品溶液为参比溶液。4.平行操作参比溶液若显色剂、样品溶液中各组分均在设定波长下有吸收,则可采用显色剂与除待测组分外的其他共存组分混合作为参比溶液。三、参比溶液
§4.4紫外-可见分光光度法的应用定性分析定量分析应用光谱对照特征数据比较吸光度比值的比较单一组分的测定多组分的测定
一、定性分析1.光谱对照同样条件下测定待测物和标准物的吸收光谱,如果两者吸收光谱一样,可认为是同一物质。如无标准物,也可比较标准谱图集里的光谱。
2.特征数据比较最大吸收波长λmax和吸光系数,是用于定性鉴别的主要光谱数据。3.吸光度比值的比较有些物质的光谱上有几个吸收峰,可在不同的吸收峰(谷)处测得吸光度的比值作为鉴别的依据。一、定性分析
二、定量分析定量分析的依据是1.单一组分的测定(1)吸光系数法查得吸光系数后根据吸光度求得样品浓度
例4-5已知维生素B12在361nm处的百分吸光系数为207。精密称取样品30.0mg,加水溶解后稀释至1000mL,在该波长处用1.00cm吸收池测定溶液的吸光度为0.618,计算样品溶液中维生素B12的质量分数。解:已知A=0.618=207l=1.00cm由A=klc样品中维生素B12含量为二、定量分析
1.单一组分的测定(2)标准比对法相同条件下,分别配制待测溶液X和标准溶液S,并分别测定吸光度。根据郎伯-比尔定律,可写出二、定量分析
例4-6为测定维生素B12原料药含量,准确称取试样25.0mg,用蒸馏水溶解后,定量转移至1000ml容量瓶中,加蒸馏水至刻度后,摇匀。另称取同样重量的B12标准品,用蒸馏水溶解后,稀释至1000ml,摇匀。在361nm波长处,用1cm比色皿分别测得样品溶液和标准品溶液的吸光度分别为0.512和0.518。求试样中B12的百分含量。解:已知Ax=0.512As=0.518两溶液配制、稀释方法一致二、定量分析
1.单一组分的测定(3)标准曲线法用标准曲线法测铁的浓度为例:①配一系列浓度的标准铁溶液,依次测定吸光度②作c-A图,即标准曲线三磺基水杨酸合铁配合物波长420nm③将待测溶液吸光度AX代入标准曲线,读出浓度二、定量分析
2.多组分的测定当溶液内有两个及以上组分并需测得各自含量时,就是多组分的测定。(1)吸收光谱互不重叠(2)吸收光谱部分重叠(3)吸收光谱相互重叠二、定量分析
2.多组分的测定(1)吸收光谱互不重叠此种情况下可以按单组分测定的方法分别求得各个组分浓度二、定量分析
2.多组分的测定(2)吸收光谱部分重叠例如右图,可先在无干扰处λ2求得a的浓度,再求得b的浓度依次求得a和b的浓度λ2处:λ1处:二、定量分析
2.多组分的测定(3)吸收光谱相互重叠解方程组法,如右图λ1处:λ2处:12解方程组可得:二、定量分析
2.多组分的测定(3)吸收光谱相互重叠等吸收双波长消去法例如右图,选取两个波长,a物质在这两波长处的吸光度相同λ1处:λ2处:二、定量分析
2.多组分的测定λ1处:λ2处:两式相减,得:在这两个波长处两组分总的吸光度的差值(⊿A)只和其中一个组分的浓度有关,可以依次求出各组分浓度。二、定量分析
1.指出下列哪种是紫外-可见分光光度计常用的光源?()B.激光器A.硅碳棒D.卤钨灯C.空心阴极灯很遗憾,您答错了答对了!点此进入下一题很遗憾,您答错了很遗憾,您答错了课堂练习
2.在一定波长处,用2.0cm吸收池测得某样品溶液的百分比透光率为71%,若改用3.0cm吸收池时,该溶液的吸光度A为()A.0.10B.0.37C.0.22D.0.45很遗憾,您答错了答对了!点此进入下一题很遗憾,您答错了很遗憾,您答错了课堂练习
3.常见紫外-可见发光光度计的波长范围为()A.200~400nmB.400~760nmC.200~760nmD.400~1000nm很遗憾,您答错了答对了!点此进入下一题很遗憾,您答错了很遗憾,您答错了课堂练习
4.测定一系列浓度相近的样品溶液时,常选择的测定方法为()B.标准对比法A.标准曲线法C.绝对法D.解方程计算很遗憾,您答错了答对了!点此进入下一题很遗憾,您答错了很遗憾,您答错了课堂练习
5.在分光光度法中,运用朗伯-比尔定律进行定量分析采用的入射光为()A.白光C.可见光B.单色光D.紫外光很遗憾,您答错了答对了!点此进入下一题很遗憾,您答错了很遗憾,您答错了课堂练习
6.许多化合物的吸收曲线表明,它们的最大吸收常常位于200─400nm之间,对这一光谱区应选用的光源为()B.能斯特灯A.氘灯或氢灯C.钨灯D.空心阴极灯灯很遗憾,您答错了答对了!点此进入下一题很遗憾,您答错了很遗憾,您答错了课堂练习
7.双波长分光光度计和单波长分光光度计的主要区别是()B.单色器的个数A.光源的个数D.单色器和吸收池的个数C.吸收池的个数很遗憾,您答错了答对了!点此进入下一题很遗憾,您答错了很遗憾,您答错了课堂练习
8.符合朗伯-比尔定律的有色溶液稀释时,其最大吸收峰的波长位置()A.向长波方向移动B.向短波方向移动C.不移动,但最大吸收峰强度降低D.不移动,但最大吸收峰强度增大很遗憾,您答错了答对了!点此进入下一题很遗憾,您答错了很遗憾,您答错了课堂练习
9.在符合朗伯特-比尔定律的范围内,溶液的浓度、最大吸收波长、吸光度三者的关系是()A.增加、增加、增加C.减小、增加、减小B.减小、不变、减小D.增加、不变、减小很遗憾,您答错了答对了!点此进入下一题很遗憾,您答错了很遗憾,您答错了课堂练习
10.在紫外可见分光光度法测定中,使用参比溶液的作用是()B.吸收入射光中测定所需要的光波A.调节仪器透光率的零点D.消除试剂等非测定物质对入射光吸收的影响C.调节入射光的光强度很遗憾,您答错了答对了!点此进入下一题很遗憾,您答错了很遗憾,您答错了课堂练习
11.在比色法中,显色反应的显色剂选择原则错误的是()A.炽热固体发射的结果C.显色剂的值愈小愈好B.显色剂的值愈大愈好D.显色反应产物和显色剂,在同一光波下的值相差愈大愈好很遗憾,您答错了答对了!点此进入下一题很遗憾,您答错了很遗憾,您答错了课堂练习
12.常用作光度计中获得单色光的组件是()A.光栅(或棱镜)+反射镜C.光栅(或棱镜)+稳压器B.光栅(或棱镜)+狭缝D.光栅(或棱镜)+准直镜很遗憾,您答错了答对了!点此进入下一题很遗憾,您答错了很遗憾,您答错了课堂练习
13.某药物的摩尔吸光系数()很大,则表明()A.该药物溶液的浓度很大B.光通过该药物溶液的光程很长C.该药物对某波长的光吸收很强D.测定该药物的灵敏度不高很遗憾,您答错了答对了!很遗憾,您答错了很遗憾,您答错了课堂练习
谢谢!'
您可能关注的文档
- 分光光度法复习题.doc
- 紫外-可见分光光度法练习题.doc
- 紫外可见分光光度法的原理与应用_.ppt
- gb1215389锅炉用水和冷却水分析油的测定紫外分光光度法.doc
- 实验二火焰原子吸收分光光度法.ppt
- 紫外可见分光光度法测定水杨酸的含量.doc
- 环境监测 基础篇 作者课件分光光度法.ppt
- 基础化学 教学课件 作者 吴华 董宪武 主编 刘强 副主编 上官少平 主审第十章分光光度法.ppt
- 无机与分析化学 教学课件 作者 王英健 尹兆明 主编第10章 分光光度法和气相色谱法.ppt
- 仪器分析 第三版课件 教学课件 作者 黄一石 吴朝华 杨小林 编 子模块4:原子吸收分光光度法任务2:原子吸收基本操作.ppt
- 仪器分析 第三版课件 教学课件 作者 黄一石 吴朝华 杨小林 编 子模块4:原子吸收分光光度法任务3:工作曲线法测定水中镁.ppt
- 仪器分析 第三版课件 教学课件 作者 黄一石 吴朝华 杨小林 编 子模块2:紫外-可见分光光度法任务3-工作曲线法定量分析.ppt
- 仪器分析 第三版课件 教学课件 作者 黄一石 吴朝华 杨小林 编 子模块2:紫外-可见分光光度法任务4:分析测试条件的选择.ppt
- 分析化学 教学课件 作者 谢美红 李春 主编第九章 紫外-可见分光光度法.ppt
- 异烟酸-巴比妥酸分光光度法测定水中氰化物的改进-论文.pdf
- COD快速消解分光光度法.doc
- 原子吸收光谱法或原子吸收分光光度法.ppt
- 分析化学第13章原子吸收分光光度法.pdf